|
|
||
|
Das Zentralatom
(Z) ( Lewis Säure = Elektronenpaarakzeptor ) ist meist ein Kation,
das häufig von Übergangsmetallen gebildet wird. Das
Zentralatom bzw. Zentralion bindet über koordinative Bindung die Liganden (Lewis Basen = Elektronenpaardonatoren
), d.h. Liganden stellen Elektronenpaare zur Verfügung, um mit dem Zentralatom
Bindungen einzugehen.
Man
nennt Komplexe deshalb auch Koordinationsverbindungen. Eine
Atombindung ( kovalente Bindung ) oder ionische Bindung
wird dagegen, bei möglichst geringer Energie,
homolytisch gespalten. |
||
|
Bsp.:
Koordinativen Bindung
|
||
|
Symbol:
b b bbbbbbbb
|
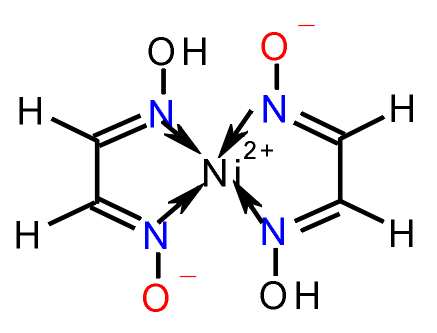
Bsp.:
Nickelglyoxim
|
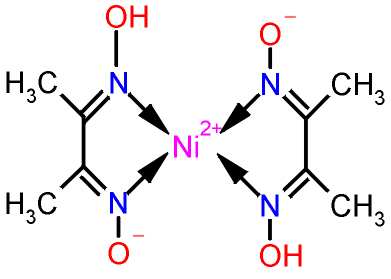
Bsp.:
Nickeldiacetyldioxim
(3D-Modell) |
 |
 |
 |
